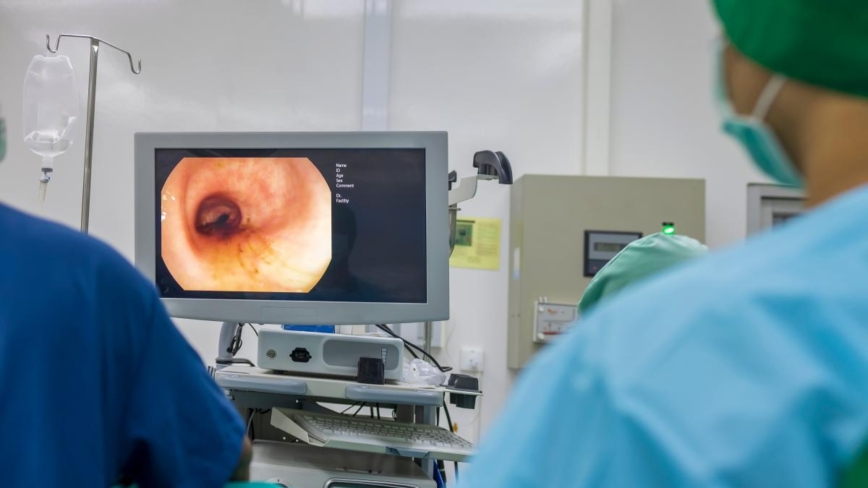
【新唐人北京时间2024年08月07日讯】美国食品和药物管理局(FDA)于7月29日批准的一项新型血液测试方法,用于结直肠癌筛查,但它也存在一些局限性。专家指出,重要的是要全面考虑所有筛检选项。
结肠癌是美国第二大致命癌症,专家长期呼吁符合条件的成年人定期进行筛检。然而,许多人因为筛检过程不舒服、侵入性强及耗时而避免这一检测。因此,FDA批准首个血液筛检选项的消息格外引人注目,这使得人们可以像检查胆固醇和血糖一样,进行结肠癌检测。
这项名为Shield的测试,需要医疗专业人员采血后送至实验室进行。它能够检测血液中的结直肠癌迹象,包括与结肠癌相关的蛋白质和肿瘤细胞DNA。自2022年起,Shield在美国已经可以透过处方使用,而现在获得FDA的批准,意味着这种筛检方法更有可能获得私人保险和Medicare的报销。
早期发现结肠癌能显着提升患者的存活率。如果在癌症仅局限于结肠时将其切除,大约有91%的患者能存活五年或以上。相反地,若癌症扩散后才被发现,仅有15%的患者能活五年以上。然而,在早期阶段被诊断出来的美国患者仅占35%。
由于结肠癌筛检能有效促进早期发现,美国预防服务工作组(U.S. Preventive Services Task Force)在几年前将建议的筛检起始年龄从50岁降至45岁,适用于平均风险群体。但研究指出,只有约三分之二的美国人遵循了这项筛检建议。
据Shield的生产商Guardant Health表示,部分人士因为不喜欢耗时且可能带来不适的结肠镜或弹性乙状结肠镜检查——后者仅检查下段肠道——而避免接受检查,这些检查都需要事先进行肠道清洁,或者需要处理粪便检查的样本。
“对于那些符合筛查指南但目前尚未进行筛查的人来说,这样的血液检查很可能会受到欢迎,”耶鲁癌症中心的医学肿瘤专家Michael Cecchini表示。他指出,这项检测对于美国及全球那些缺乏结肠镜等侵入性检查设施的地区尤其重要。
不过,Cecchini也强调,需要进行更多研究来确认,从长期来看,这种血液检查是否能够降低结肠癌的死亡率,这是研究者追求的目标。
结肠镜仍不可或缺
FDA的批准是在3月《新英格兰医学杂志》发表了一项涵盖全国城乡社区超过20,000人的临床试验后作出的。该试验显示,Shield血液筛检能正确识别出83%的结直肠癌患者,这一准确率略低于粪便DNA测试。
然而,Shield未能检测出许多大型息肉,部分息肉可能最终转化为癌症。
Cecchini表示:“从另一角度来看结肠镜等其它筛检方法,不仅能发现癌症,还能切除癌症前期病变的息肉。”
此外,血液筛检结果呈阳性的患者仍需接受结肠镜检查以确认结果非假阳性,这种情况约占10%。
值得担忧的是,保险公司可能不会像对待常规结肠镜检查那样,依法全额支付血液测试呈阳性后的结肠镜检查费用。
但根据经验,这可能不是问题。佛罗里达州博卡拉顿的胃肠科医生Prosper Abitbol表示,“在 Cologuard粪便DNA测试呈阳性后,保险公司已经支付了筛检结肠镜检查的费用。”
专家指出,选择合适的筛查方案是至关重要的。
在美国,45至75岁或以上且大肠癌风险约为平均值的人士,应该每10年接受一次被视为黄金标准的结肠镜检查;或每五年进行一次柔性乙状结肠镜或虚拟结肠镜检查;或每三年做一次粪便DNA测试;或每年进行其它粪便检查;或尝试新的血液检测。
目前尚不明确Shield测试应该多久进行一次,因为它还没有被纳入癌症筛查的官方指南。纽约大学格罗斯曼医学院的胃肠病专家Aasma Shaukat表示,评估不同间隔以准确确定最理想的时间“大概需要10年的时间”,她曾参与制定胃肠病学会的筛查指南。“在那之前,制造商很可能会推荐保险公司愿意支付的间隔,就像目前对Cologuard的做法一样,”Shaukat说。
Cecchini认为,虽然血液检测可能不如其它方法全面,但其操作简便是一大优点。“最佳”的筛查测试是患者愿意接受的那一种。
(转自大纪元/责任编辑:叶萍)